La vacuna contra el coronavirus de Pfizer costará US$ 20 ,anunciaron Inc. y BioNTech que comenzaron un ensayo de fase…
vacuna
Ginés González: “Estamos negociando la prioridad en la asignación de vacunas a la Argentina”.El ministro de Salud se mostró optimista…
Todas las dosis se encuentran en prueba, por lo que todavía es difícil poder definir su valor de venta. Estiman…
Este lunes comenzó el primer ensayo clínico de fase 3 de una vacuna contra el coronavirus en Estados Unidos. La…
El ministro de Defensa, Agustín Rossi, explicó que «ya hay más de 15.000 voluntarios anotados» para someterse a pruebas de…
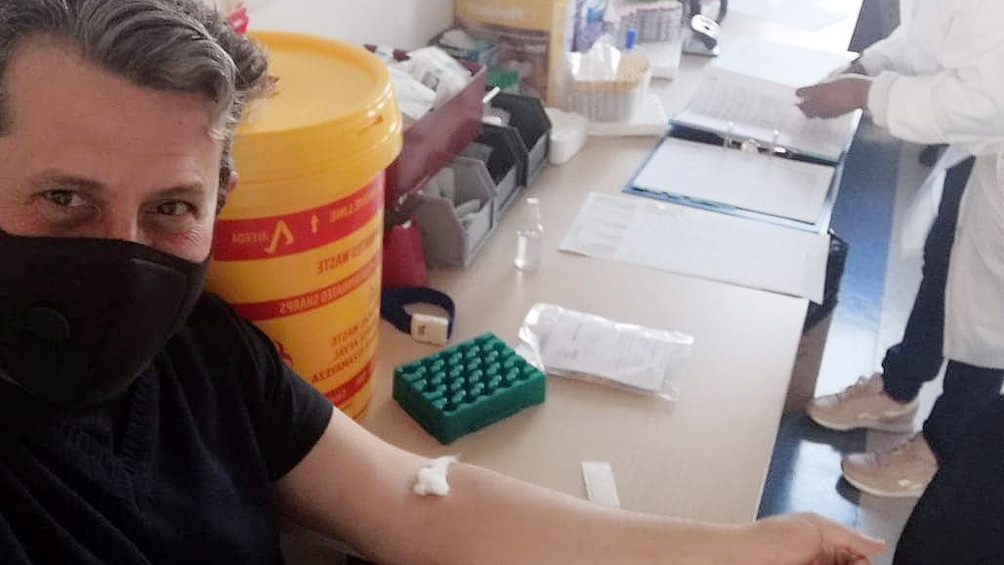
Argentino que recibió la vacuna contra el coronavirus dice:»Los médicos están entusiasmados».Nacido en Lomas de Zamora, pero criado en Santiago…
China concederá un crédito de 1.000 millones de dólares para que los países de América Latina y el Caribe puedan…
Una vacuna contra el coronavirus desarrollada por la biofarmacéutica china CanSino Biologics y la unidad de investigación militar del país…
Unas 20.000 dosis de la vacuna experimental de la compañía privada china Sinovac Biotech llegaron hoy a San Pablo para…
Los ensayos realizados en fase 1 y 2 en alrededor de 1.077 voluntarios mostraron que la posible vacuna contra el…