El Servicio Nacional de Sanidad y Calidad Agroalimentaria (Senasa) junto a las secretarías de Agricultura Familiar, Campesina e Indígena y…
tratamiento
El Banco de Sangre del HZE convoca a las personas que hayan superado el virus y tengan en el plasma…
El Intendente de Trelew, Adrián Maderna reconoció que los malos olores son un reclamo constante de los vecinos. También se…
La jueza Civil, Comercial y Laboral de Esquel, Dra. Alicia Arbilla, rechazó la Medida Autosatisfactiva promovida por el Sr. Mauricio…
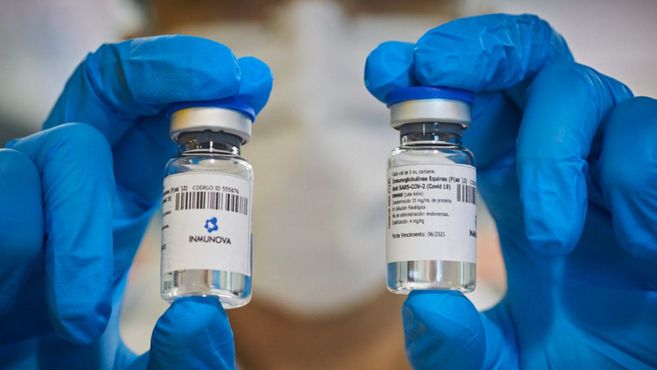
Entre las muchas opciones de tratamiento que se barajan como modo de contener la pandemia de coronavirus SARS-CoV-2, el plasma…
El periodista Sergio Lapegüe se encuentra internado por covid-19 hace 13 días y en las últimas horas compartió una foto…
La medida autosatisfactiva es para frenar el tratamiento de la zonificación minera. No a la Mina se presentó en Tribunales…
Lo apuntó Pablo Lada, integrante de la asamblea de Trelew, al referirse al nuevo embate para habilitar la megaminería. “Se…
El presidente Alberto Fernández recorrió este mediodía las instalaciones de la compañía biotecnológica Inmunova, en el campus de la Universidad…
Un tratamiento para la artritis demostró que puede reducir en un 24% el riesgo de muerte de pacientes con el…